ȫ����ҩ����������ҩ��˾��������Euronext��IPN��ADR��IPSEY���ڽ��չ�����2024��ǰ�����ȼ�2024��������ȵ�ҵ����
Ҫ��
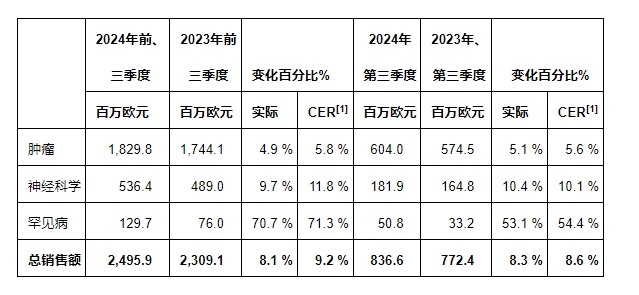
• �Թ̶�����[1]���㣬2024��ǰ�����ȵ������۶�������Ϊ9.2%����������Ϊ8.1%������������Ҫ�����������������棺����®��AbobotulinumtoxinA����Cabometyx®��Cabozantinib����Bylvay®��Odevixibat��ҵ��������������������®�������ģ����۶��Ƚ��������Լ���2L PBC[2]�����Ƴ���Iqirvo®��Elafibranor������1L mPDAC[3]�����Ƴ���Onivyde®�������濵��Ҳ����
• Iqirvo��Kayfanda®��Odevixibat����ŷ�˻�ü����
• �ϵ�2024�����ָ�����Թ̶�����[1]����������۶���������8.0%��ǰ��ָ�����Թ̶�����[1]���㳬��7.0%��������Ӫҵ�����ʸ��������۶��31.0%��ǰ��ָ��������30.0%��
��ϯִ�й�David Loew��ʾ��"��2020�����ǵ�ս����������������ʵ���˳���������������Ҳ�����⣬ͬʱ�з�����Ҳȡ�ý�һ����չ�����ǻ������Ƴ�������Ӧ֢�������ߣ�����������е�Iqirvo��Onivyde������չ˳�����ڽ���ǰ������ҵ����֧���£����ǽ���һ���ϵ�2024������۶������ָ����
�����Ѵ������õĽ�����¼�����ⲿ���¡���ҵԽ�����dz���Ϊ�����ṩ����ѡ���ʹ��Ϊ�˵춨�˼�ʵ������"
2024��ȫ��ָ��
���ڵ������ȵ�ǿ��ҵ�����������ѽ�һ���ϵ�2024��IJ���ָ����
• ���̶����ʼ��㣬�����۶������ʳ���8.0%��ǰ��ָ��������7.0%��������2024��9�µ�ƽ������ˮƽ��Ԥ�ƻ��ʽ��������۶����Լ1.5%�IJ���Ӱ��
• ����Ӫҵ�����ʸ��������۶��31.0%��ǰ��ָ��������30.0%��
�з����߸���
2024��9�£�Iqirvo 80 mgƬ�������ŷ��ίԱ��ĸ�����������������ȥ�����ᣨUDCA���������ƶ�UDCAӦ����ij��˻��ߵ�PBC������������UDCA�Ļ�����������ҩ���ơ�2024��6�£�Iqirvo����ͬ�����»��������FDA������
2024��9�£�ŷ��ίԱ�ỹ��Kayfanda��������Alagille�ۺ�����ALGS�������仼����������Odevixibat����Ʒ��ΪBylvay���ѻ������У���ŷ���������ƽ����Լ����Ը��ڵ�֭�ٻ���PFIC������������ŷ����������PFIC����������������ALGS��
ͬ�£�CABINET ������������ս����2024��ŷ�������ڿ�ѧ�����Ϲ��������ڡ���Ӣ����ҽѧ�ڿ����Ϸ�������һ��֤ʵ��Cabometyx�����������ڷ�����������Ч���档��ʱ����������������ŷ��ҩƷ�������ύ�������ɵ�������Ӧ֢���롣
ҵ��չ
2024��8�£�������ǩ��Э�飬�����亱�����Ƽ�����������ȯ����ΪЭ���һ���֣��������ڵ��������յ�1.58����Ԫ���ֽ�֧����
2024��10�£�Eton Pharmaceuticals�����������Э�飬�չ�Increlex®��Mecaserminע��Һ����Ԥ�Ƹý�����2024�����ǰ��ɡ�
��Galderma���ٲó���
����2024��9��30�գ�Galderma�ڹ����̻ᣨICC��������������������ٲó������ڽ����С���һ��������Galderma��2021�귢���漰����2007����ŷ�ˡ�ijЩ��ŷ���Һ�����ǩ���Э������Azzalure®��AbobotulinumtoxinA���ͼ�����ص���ҵ����ϵ�ĵ���Χ��ICC�ڲ��ٲ�ͥ��2024��10�·������ղþ�������Galderma�ڵ�һ���ٲ��еĴ֣��������ȫ�������⣬��Ҫ��Galderma�е������������Ĵַ��ɷ��ú��ٲ÷��á�
�ڶ���������Galderma��2023��11�·����漰������2023����ֹ˫����2014����ݸ��Ե�����������Ŀ������IPN10200������ǩ���������з�����Э�����Ч�ԡ����ֽΣ�������������Ԥ����һ����ʣ���ٲó�����κ�DZ�ڲ���Ӱ�죬�����������ֺ�����ά����Ȩ����
˵��
���в������ݾ�����ŷԪ��€m��Ϊ��λ���������ҵ������2024��9��30��֮ǰ��9���£�2024��ǰ�����ȣ���2024��9��30��֮ǰ��3���£�2024��������ȣ������������ݶԱȵĶ���Ϊ2023��9��30��֮ǰ��9���£�2023��ǰ�����ȣ���2023��9��30��֮ǰ��3���£�2023��������ȣ�����������˵�����������ۻ���2024��ǰ�����ȵ�ҵ����
����������
��������һ��ȫ���Ե�������ҩ��˾��רע��������������������ѧ������������Ϊ�����ṩ������ҩ����ǵ��з��������ⲿ����Ϊ�������н�����Ŀ��������Լ�������������Ӣ����ȫ��������Ϊ������֧�֡��ֲ���40������ҵ�ȫ���Ŷӣ���ͬ��������������صĺ�������ϵ��ʹ����Ϊ100������ҵĻ����ṩҩ�
�������ڰ��裨��ŷ��������IPN�����в�ͨ��������I����������ƾ֤��Ŀ��ADR��IPSEY�����������н��ס�
�����������й�
������������1992������й���2019�����Ϻ������������ģ���ȫ���ĸ��з�����֮һ����������2021�����Ϻ������й����ܲ�������2022����ݼ���ҵ��䶯��ͬ�������Ԫ����ҵ��רע����ҩ�������������������������������ѧ��Я���Ϻ��������ij����Ƴ��������Ʒ����������й�����ؽ���������������
������-�й�ǰհ�������ľ�ʾ˵��
��������ǰհ��������Ŀ�ĺ�Ŀ����ڼ��ŵĹ���ս�ԡ���ǰ�۵�ͼ��衣���������漰��֪��δ֪�ķ��պͲ�ȷ���ԣ����ܵ���ʵ�ʽ����ҵ�����¼��뱾����Ԥ�ڵĴ���ͬ���������з��վ�����Ӱ�켯����δ��ʵ�������Ŀ�������������Ŀ���ǻ����ֽ������Ϣ�ں����ĺ�۾����������趨�ġ�"����"��"����"��"�ڴ�"�ȴ�������Ʊ�����ʹ����Ϊ����ȷǰհ���������������Ŷ�δ���¼��������������¼���������ļ��;��������⣬��������Ŀ����ƶ�δ�����ⲿ���������DZ��δ���չ����������߿��ܻ�ʹָ�귢���仯��Ŀ�ĵ������Ǽ�����Ϊ���������ݺͼ��衣Ŀ��ȡ���ڽ������ܷ�������������ʵ��������ȡ������ʷ���ݡ����ǵ�ijЩ���պͲ�ȷ���Եķ�����ʵ�ʽ����������Щָ���кܴ���룬���Ա���Ϊ�������з��λ��ٴ���������ǰ���IJ�Ʒ����������Զ����Ͷ���г���ﵽ����ҵĿ�꣬����������ע�����ԭ���ű�����Ի����������Է���ҩ�ľ���������ܻ�ת��Ϊ�г��ݶ����ʧ�����⣬�з������漰����Σ�ÿ���ζ��漰�ش���գ������ſ�����ʵ����Ŀ�IJ����ȷ�����������Ͷ������ʽ�IJ�Ʒ������Ŭ������ˣ����Ų���ȷ�����ٴ�ǰ�����л�õ���������Ƿ���������ٴ������еõ�ȷ�ϣ�Ҳ����ȷ���ٴ�����Ľ���Ƿ�����֤����ز�Ʒ�İ�ȫ�Ժ���Ч�ԡ����ܱ�֤��Ʒ����ñ�Ҫ��ע������ò�Ʒ����֤������ҵ���dzɹ��ġ������������֤����ȷ��ȷʵ���ַ��ջ�ȷ���ԣ���ʵ�ʽ��������ǰհ�������еĽ���кܴ�ͬ���������պͲ�ȷ��������������һ����ҵ�����;�����һ�㾭�����أ��������ʺͻ��һ��ʲ�������ҩ��ҵ�����ҽ�Ʊ���������Ӱ�죻ȫ��ҽ�Ƴɱ��������ƣ��������ֻ�ü����������²�Ʒ��ר�����²�Ʒ�з��й��е���ս��������ü�ܲ��ŵ���������ȷԤ��δ���г�״�����������������ѻ������ʾ��õĽ��ڲ��ȶ�����Ȩ���գ��Լ���ר������Ч�Ժʹ��²�Ʒ�������������������Լ��������ٵ����ϣ�����ר�����Ϻ�/�������ϡ����⣬�����������������з�������ijЩ��Ʒ����Щ��Ʒ���ܻ�����������Ȩʹ�÷��ã���Щ����������Ϊ���ܻ�Լ��ŵĻ�Ͳ�������������Ų���ȷ���������齫���и��Ե������ſ���������ЩЭ���л���κ����档�����κκ������ΥԼ�����������Ԥ�ڵ����档����������ܻ�Լ��ŵ�ҵ����״����ҵ����������Ӱ�졣������ȷ�������������÷�������Ҫ�����䲻�е����»��������Ÿ������������κ�ǰհ��������Ŀ��������κ������Է�ӳ�������������ݵ��¼��������������������κα仯��Ҳ����ʹ������κγ�ŵ�����ŵ�ҵ�����������ڷ��������г���ܻ���������ע���ļ��и����ķ������ء����ļ������з��պͲ�ȷ���Բ����꾡���ţ�������߲��ļ�����վ�ϼ��ŵ�����ͨ��ע���ļ���
[1]�Թ̶����ʣ�CER�����㣬��ͨ��Ӧ��ǰһʱ��ʹ�õĻ������¼������ʱ�ڵ�ҵ�����ų��κ����Ӱ�졣
[2]ԭ���Ե�֭�Ե����������ơ�
[3]ת�������ٵ����ٰ�һ�����ơ�
����Ȩ�������������ɵ��������������ݼ�ͼƬ����Ϊ�������뱾��վ�ء����ĵ�ԭ�����Լ����г������ֺ۵�δ����վ֤ʵ���Ա����Լ�����ȫ�����߲������ݵ���ʵ�ԡ������ԡ���ʱ�Ա�վ�����κα�֤���ŵ������߽����ο���ת�ش����dz��ڴ��ݸ�����Ϣ֮Ŀ�ģ���������������ͬ��۵�Ͷ�����ʵ�Ը���������ֱ�վ�����ӳ�Ϯ�����ݣ����ṩ���֤�ݣ�һ����ʵ����վ������ɾ��������Ȩ���ݡ�